この記事を読んでわかること
・Summit therapeuthics(サミットセラピューティクス)についての概略と今後の日本展開(予想)
*この記事ではアフィリエイト広告を掲載しています。
どうも、こんにちは。外資系製薬会社経営企画室に勤めるこういちです。
今日はSummit therapeutics(サミットセラピューティクス)を取り上げます。

2026年のJSMO 日本臨床腫瘍学会でもスポンサード企業として広告掲載していた企業です。
https://www.congre.co.jp/jsmo2026
学術集会のTop Pageで、広告が掲載されているので目にした方も多いかと思います。
Xでも少し話題になっていましたね。
ということで調べてみました。
私自身は肺がん領域に詳しくないので、生成AIの力を借りながら色々調べました。
今日はその情報をお伝えしますね。
いま動いている臨床試験がすべて成功したら、かなりポテンシャルのある企業だと感じたので、今日はその辺りについて解説します。
まずは第1部で、AIにまとめてもらった情報をFactベースでお届けします。
第2部は、私の所感とこの企業のポジション探しについて個人的な考えを述べていきます。
それではどうぞ。
第1部:AIによる会社情報ならびに精緻な技術・財務・市場解説(最新エビデンス準拠)
Summit Therapeuticsの歴史:死地からの復活劇
Summit社の歴史は、まさに波乱万丈です。もともとはデュシェンヌ型筋ジストロフィー(DMD)やCDI(クロストリジウム・ディフィシル感染症)の治療薬を開発していましたが、臨床試験の失敗が続き、一時は株価が1ドルを割り込む「ペニーストック」の状態にありました。
転機となったのは、現CEO兼会長であるRobert W. Duggan(ボブ・ダガン)氏の就任です。彼はかつてファーマサイクリックス社(BTK阻害薬のインブルビカを開発)をアッヴィへ210億ドルで売却した伝説の経営者。彼が目をつけたのが、中国のAkeso(康方生物)が開発していたイボネシマブでした。
このイボネシマブですが、キートルダーを上回る効果が2024年に確認され、一気に注目の的になりました。
このイボネシマブの承認がいよいよ、26年の後半に迫っている、というのがいまの状況です。
米国承認目標日(PDUFA date):2026年11月14日の米国承認目標日
- 本社: 米国フロリダ州マイアミ(2024年にカリフォルニアから移転)
- 主要パイプライン: Ivonescimab (PD-1/VEGF bispecific antibody)
- 戦略的提携: 2022年、Akeso社から米国、カナダ、欧州、日本における独占的権利を最大50億ドル(契約一時金5億ドル)で獲得。
企業概況と財務ハイライト:2026年2月決算報告(Form 10-K)
2026年2月23日に発表された2025年通期決算報告に基づき、Summit社の現在の財務体質を解剖します。
強固なキャッシュポジション: 2025年12月31日時点の現金および現金同等物は約7億1,340万ドル。前年の約4.12億ドルから大幅な積み増しに成功しています。これは、グローバル第III相試験を自社主導で完遂するための十分な資金力を示しています。
開発投資の加速: 2025年の純損失は約10.79億ドル。この巨額の「赤字」は、イボネシマブのグローバル治験費用、および将来の商用化に向けたインフラ構築、さらにトップタレント獲得のための報酬によるものです。バイオテック特有の「将来への先行投資」が結実しつつあります。
戦略的パートナーシップ: 2026年1月、Summit社はGSK社との臨床試験提携を発表。GSKのB7-H3標的ADC「risvutatug rezetecan」とイボネシマブの併用試験を2026年中盤より開始する予定です。
参照元:
- Summit Therapeutics Inc. “Reports Financial Results and Operational Progress for the Fourth Quarter and Year Ended December 31, 2025” (Feb 23, 2026)
- URL:https://smmttx.com/news/press-releases/news-details/2026/Summit-Therapeutics-Reports-Financial-Results-and-Operational-Progress-for-the-Fourth-Quarter-and-Year-Ended-December-31-2025/default.aspx
核心薬イボネシマブ(Ivonescimab):サイエンスの勝利
イボネシマブ(ivonescimab)は、PD-1とVEGFの両方を標的とする、世界初の二重特異性抗体(Bispecific Antibody)です。
- 作用機序(MOA): VEGFが高発現している腫瘍微小環境において、PD-1への結合親和性が劇的に高まる「四価結合」の設計。これにより、全身への副作用を抑えつつ、腫瘍部位で集中的に免疫を活性化させます。血管新生阻害と免疫チェックポイント阻害の相乗効果を、1つの分子でパッケージ化しています。
参照元:
- Summit Therapeutics “Ivonescimab: A Potential First-in-Class Bispecific Antibody”
- URL:https://www.smmttx.com/pipeline/ivonescimab/
【MOA深掘り解説】イボネシマブの革新性:なぜ「四価結合」が劇的な効果を生むのか
イボネシマブの最大の特徴は、単一の分子にPD-1とVEGFという2つの異なる標的への結合部位を持たせた「二重特異性(Bispecific)」かつ「四価(Tetravalent)」の構造にあります。この設計が、腫瘍微小環境(TME)においてどのようなマジックを起こしているのか、3つのポイントで解説します。
①結合親和性の「協調的」強化(四価結合のロジック)
通常の抗体は二価(結合部位が2つ)ですが、イボネシマブはPD-1に2つ、VEGFに2つの計4つの結合部位を持つ四価構造です。 ここで重要なのが、「VEGFとの結合がPD-1への結合をブーストする」という協調的な特性です。
- 物理的な繋ぎ止め: 腫瘍組織内では、血管新生が活発なためVEGFが高濃度で存在します。イボネシマブがまずVEGFに結合することで、分子が腫瘍組織内に「係留(アンカー)」されます。
- アビディティ(多価結合親和性)の向上: 係留された状態で周囲のT細胞上のPD-1を探索するため、結合の確率と強度が飛躍的に高まります。データによれば、VEGFが存在する環境下では、PD-1への結合親和性が10倍以上に向上することが示されています。
②腫瘍微小環境の正常化と免疫活性の「同期」
がん細胞はVEGFを放出することで、自身の栄養源となる血管をでたらめに作り出し(血管新生)、同時に免疫細胞が働きにくい「酸性・低酸素・高圧」なバリアを形成しています。
- バリアの破壊: イボネシマブがVEGFを阻害することで、異常な血管構造を整理・正常化させます。これにより、腫瘍内部の圧力が下がり、免疫細胞が内部へ浸透しやすい「通り道」が作られます。
- ワンストップ・デリバリー: 血管を正常化したまさにその場所で、同時にPD-1をブロックしてT細胞を活性化させます。つまり、「敵の城壁を壊す(VEGF阻害)」と「味方の兵を突撃させる(PD-1阻害)」を、同じ場所・同じタイミングで完璧に同期させているのです。
③「オン・ターゲット、オフ・腫瘍」の副作用低減
従来のPD-1阻害薬とVEGF阻害薬の「カクテル(併用)療法」では、全身の血管や正常組織にも両方の薬剤が作用するため、出血や高血圧、自己免疫疾患様の副作用が重畳しやすいのが難点でした。
- 選択的活性化: イボネシマブの四価設計は、VEGF濃度が低い正常組織ではPD-1への結合力が相対的に弱まるようチューニングされています。
- 安全性の担保: これにより、「腫瘍という戦場では最強、それ以外では静か」という、理想的な標的選択性を実現しています。これが、臨床試験において高い有効性を示しながらも、管理可能な安全性プロファイルを維持できている科学的背景です。
参照元:
- Akeso Inc. “Scientific Rationale for Ivonescimab (AK112): A Potential Best-in-Class PD-1/VEGF Bispecific Antibody”
- URL:https://www.akesobio.com/en/pipeline/ak112/
- Gu L, et al. “A novel PD-1/VEGF bispecific antibody (AK112) exhibits potent anti-tumor activity.” Journal of Clinical Oncology. 2022; 40(16_suppl): 2548.
臨床エビデンスの検証(Lancet掲載データ)
Summit社の価値を決定づけたのは、医学誌 The Lancet に相次いで掲載されたデータです。
HARMONi-2(対キイトルーダ直接対決)
進行NSCLC(PD-L1陽性)の1次治療において、イボネシマブ単剤がキイトルーダ(pembrolizumab)単剤に対し、無増悪生存期間(PFS)の中央値を11.14ヶ月 vs 5.82ヶ月と劇的に改善しました。
- ハザード比(HR): 0.51(95% CI: 0.38-0.69, p<0.0001)。
参照元:
- Zhou C, et al. “Ivonescimab versus pembrolizumab in high-expressed PD-L1-positive NSCLC: a phase 3, randomised, double-blind study (HARMONi-2).” The Lancet. 2024; 404(10457): 1029-1039.
- URL:https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(24)01915-1/fulltext
HARMONi-A(EGFR変異陽性例)
第3世代EGFR-TKI(タグリッソ等)投与後の難治例において、死亡リスクを26%減少(HR: 0.74, p=0.019)させ、OS(全生存期間)の有意な改善を示しました。最新の2026年3月ELCC(欧州肺癌学会)での発表では、脳転移を有する患者に対しても優れた脳内PFS改善(HR: 0.72)が示されています。
参照元:
- Yang Y, et al. “Ivonescimab plus chemotherapy in EGFR-mutant NSCLC after progression on EGFR tyrosine kinase inhibitors: a phase 3, randomised, double-blind study (HARMONi-A).” The Lancet. 2024; 403(10444): 2612-2626.
- URL:https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(24)01016-2/fulltext
日本における進行中の臨床試験情報
Summit社は日本を含む様々な国、地域での開発を加速させています。
日本においては、JRCT上で、2026年4月19日現在3つの試験が動いているのを確認しました。
これはAIに頼らず自分で調べました。
以下その写真です。
Ivonescimabで検索したら3つの試験がヒットしました。
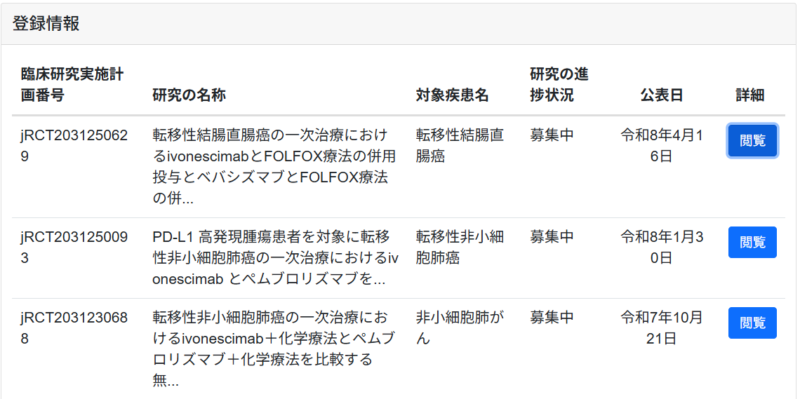
- HARMONi-3試験(NCT05899608): 1次治療の転移性NSCLC(扁平上皮・非扁平上皮)を対象に、イボネシマブ+化学療法 vs キイトルーダ+化学療法を比較。日本国内の複数の医療機関でも症例登録が進んでおり、2026年第2四半期には扁平上皮コホートの中間PFS解析が予定されています。
→日本のJRCT情報はこちら
転移性非小細胞肺癌の一次治療におけるivonescimab+化学療法とペムブロリズマブ+化学療法を比較する無作為化二重盲検国際共同第III相試験(HARMONi-3試験)
https://jrct.mhlw.go.jp/latest-detail/jRCT2031230688
HARMONi-7試験(NCT06767514): PD-L1高発現(TPS≧50%)のNSCLC 1次治療における、イボネシマブ単剤 vs キイトルーダ単剤の直接比較。これもグローバル試験として日本での展開が予定されています。
→日本のJRCT情報はこちら
PD-L1 高発現腫瘍患者を対象に転移性非小細胞肺癌の一次治療におけるivonescimab とぺムブロリズマブを比較する無作為化二重盲検多地域共同第 3 相試験(HARMONi-7 試験)
https://jrct.mhlw.go.jp/latest-detail/jRCT2031250093
HARMONi-GI3試験(NCT06684743)2025年第4四半期に開始され、標準治療に抵抗性を示す転移性大腸がん患者を対象に、イボネシマブ+化学療法の有効性と安全性を検証しています。肺がんで示された高い腫瘍特異性とVEGF阻害による微小環境の正常化が、消化器がんでも再現されるかが焦点です。
→日本のJRCT情報はこちら
https://jrct.mhlw.go.jp/latest-detail/jRCT2031250629
転移性結腸直腸癌の一次治療におけるivonescimabとFOLFOX療法の併用投与とベバシズマブとFOLFOX療法の併用投与を比較する無作為化、実薬対照、二重盲検、多施設共同、第3相試験(HARMONi-GI3)
第2部:こういちの所感とSummit社の求人に関して
こういちの所感
ここまでFactを中心に見てきました。
基本AIで調べた情報を元に、私自身でも日本の臨床試験情報などを調べてみました。
間違っている箇所があったらすみません。引用を入れて、Fact Checkもしたので大丈夫だと思いますが、間違いに気づいた方がもしいらっしゃればご指摘頂ければと思います。
さて、中国ですでに発売していることも情報として掴んだので、どれくらい売れているか気になりました。
またまたAI調べにはなりますが、その情報も以下に載せておきます。
1. 売上高:1年で約630億円規模へ急成長
Akeso社が2026年3月26日に発表した「2025年度通期決算報告」により、以下の数値が確定しています。
年間製品売上高: 30億3,310万人民元(約630億円)
- 成長の原動力となっているのがイボネシマブです。2024年5月に中国で承認されて以降、ものすごいスピードで市場に深く浸透しています。
- 成長率: 前年比で51.48%増という驚異的な伸びを記録。
- https://www.akesobio.com/en/media/akeso-news/260327/
- NRDL(国家医療保険カタログ)への収載: 中国での売れ行きを左右する最大の要因である「国家保険」に速やかに収載されたことで、患者の自己負担が激減し、処方数が爆発的に伸びています。
2. 「キイトルーダ超え」の衝撃が現場を動かしている
中国国内で行われたHARMONi-2試験(キイトルーダとの直接対決)の結果が、現場の医師の処方行動を劇的に変えました。
- SoC(標準治療)の交代: 中国の腫瘍内科医の間では、PD-L1陽性の肺がんにおいて「キイトルーダよりもイボネシマブ」という選択が急速に一般化しています。
- 圧倒的なシェア: 承認から1年強で、主要な大病院(ターシャリー病院)における肺がん1次治療の新患シェアを急速に奪っており、外資系メガファーマの脅威となっています。
3. 適応拡大によるさらなるブースト
現在、中国では以下の適応で売上を伸ばしています:
- EGFR変異陽性NSCLC(TKI治療後): 最初に承認された領域。
- PD-L1陽性NSCLC(1次治療): 2024年後半に承認。これが売上の最大ボリューム層となっています。
っとここまでがAI情報です。
いやはや、これはすごいですね。
キートルーダ超え、さらに中国ですでに発売されており、驚異的なスピードで売り上げを伸ばしている。
FDAで2026年後半に承認されたら
アメリカでも爆発的に売れていくのではないかと予想します。
そうすれば日本でも同じことが起きると予想されます。
株価もいまそこまで高くないので
仕込むならいまのタイミングかもしれません。
*注意:投資は自己判断です。
投資の話はおいておくとして、この会社が日本に上陸してきたら、オンコロジーの世界観がまた変わりそうですね。
臨床腫瘍学会に参加していないのでわかりかねますが、肺がんの領域ではすでにそういったムーブメントが起こりつつあるかもしれないですね。
このあたりの情報はまた詳しい人がいたら教わりたいところです。
Summit社の求人に関して
さて、このSummit社ですが、日本人の社員も数名Linked inで発見できます。
すでに雇用が動いているのですね。
ただ日本法人の登記情報はネットで調べても、またAIに聞いても出てきませんでした。
なので、まだこれからなのかなと予想します。
ただ、臨床腫瘍学会学術集会2026のホームページのトップページに広告協賛(エビデンスURL:https://www.congre.co.jp/jsmo2026/)するくらいですので、確実に日本でビジネスを展開する考えがあるのかなと推察されます。
そうなると、面白いですよね。
完全立ち上げ案件、薬はピカ一、急成長中
こんな案件はなかなかありません。
立ち上げ時は少人数でOperationを回していくことになるので、めちゃくちゃ忙しいことが予想されますが、組織や仕組みを作っていく面白さもあると思います。
オンコロジーのバックグランドがあり、また肺がん領域にすでに知見・経験があるMRやメディカル、またマーケティング担当者にとっては非常に興味のある企業なのではないかなと、サミット社の情報を調べていて感じました。
ただ残念ながら現時点では、私自身がどこのエージェントがこの求人を掴んでいるか、わかっていません。
こういった外資バイオベンチャーのサポートをよく行っているのがJAC Recruitmentです。
日本の老舗だけあってこういった案件をたくさん持ってます。
過去、InsmedやRegeron案件も紹介してもらったことがあります。
あと、
Answersさんも、非公開の外資バイオベンチャー案件を幅広く扱っているので個人的におススメしています。
またあまり知られていないですが、
ランスタッドさんも外資には強いです。
この案件はさすがにランスタッドさんは有していないかな、と思いますが、どこのエージェントがその企業に強いかは、その時々で変わってくるので、何社かに話を聞いてみるのが良いと思います。
私自身のスタンスとして「どこどこのエージェントが一番いいです」というのは述べていません。
なぜなら、その時々でエージェントが持っている案件は異なるためです。
応募はしなくていい。ただ「情報が自動で入る仕組み」は今すぐ作ることをおすすめしてます。
サミット社の臨床試験の結果ならびに中国での爆発的成功を目の当たりにして、心が動かない製薬パーソンはいないはずです。
そしてこの薬を扱ってみたい
立ち上げフェーズの企業に参画したい
と思った人も中にはいるかもしれません。
ですが、こうしたチャンスを掴めるのは「運が良い人」ではなく「情報を網羅している人/情報を自ら探しに行っている人」だけです。
エージェントとのコミュニケーションに関して言えば、希望条件を一度伝えておけば、あとは日々の仕事に集中している間に、エージェントがあなたの代わりに市場を監視し、最適なタイミングでチャンスを知らせてくれます。
動くかどうかを決めるのは、情報を得てからで十分です。
まずは「どんな選択肢が市場にあるのか」を把握すること。このアクションの積み重ねこそが、不透明かつ早期退職の嵐が吹き荒れる製薬業界を勝ち抜く生存戦略の一つの方法です。
AnswersさんやJAC Recruitmentさん、ランスタッドさんは比較的幅広く求人を扱っているので個人的に強くおススメしています。
ということで本日のブログの内容は以上です。
最後までお読み頂きありがとうございました!






コメント