この記事を読んでわかること
・Kalvista Pharmaのパイプライン
・Kalvista Pharmaの日本の臨床試験
*この記事はアフィリエイト広告を利用しています。
どうも、こんにちは。
外資系製薬会社、経営企画室に勤めるこういちです。
さて、今日は2024年1月に日本法人が立ち上がったばかりのKalvista Pharmaの紹介です。
存在自体はうっすら知っていたものの、筆を執らずに来ましたが、X経由で連絡が入り、少し情報をまとめてみようかなと思い、いまこうして書いています。
昔、といってもブログを始めた3年前はこういう会社の情報や薬の情報を調べるのは時間が掛かっていました。
でもいまはAIがあります。
ということで、今日もその機能をふんだんに活用して、記事をまとめていこうと思います。
KalVista Pharmaceuticals とは

アメリカのマサチューセッツ州にある製薬会社になります。
概要調べる時は、AIに聞くのが一番!
ということで、回答をそのまま引用します。
KalVista Pharmaceuticalsは、遺伝性の血管浮腫(HAE)などの疾患に対する経口治療薬を開発しているバイオファーマシューティカル企業です12。
主なポイントは以下の通りです:
「KalVista Pharmaceuticalsについて教えてください。」 Copilot AI 4/4時点 一部改変
あれ?
もうちょっと会社のベーシックな情報が出るかなと思いきや、いきなり治療薬の話が出てきました。
ということで、別のソースから引用します。
法人名 : Kalvista Pharmaceuticals, Inc.
設立 : 2011年5月
代表者 : Andrew Crockett(CEO)
事業内容: Kalvista Pharmaceuticals, Inc.は、アンメットニーズが極めて高い希少疾患の治療薬として、経口投与が可能な低分子プロテアーゼ阻害薬を創薬、開発、販売する企業です。目下、HAE急性発作時の経口治療薬である、sebetralstatを日本を含む複数国にて国際共同開発を行っています。また、開発パイプラインの中には、経口投与が可能な第XII因子阻害薬があり、HAEをはじめとした複数の疾患に対する新たな治療法として期待されています。
所在地 : 米国マサチューセッツ州 ケンブリッジ
URL : https://www.kalvista.com/
「製薬企業 KalVista Pharmaceuticals, Inc. 遺伝性血管性浮腫(HAE)診断コンソーシアムに賛助会員として参画」
一般社団法人遺伝性血管性浮腫診断コンソーシアム 2023年11月01日
設立自体は2011年です。
まだ若い会社ということがわかります。
ネタバレ感も含まれる引用になってしまっていますが、すでに日本の遺伝性血管性浮腫診断コンソーシアムにも加盟済みです。
(そもそも、この会社の存在を知ったのも、このプレスリリースです。)
ということで、遺伝性血管性浮腫の治療薬を持っている武田薬品、鳥居薬品、CSLベーリングの方などはすでにご存じの会社さんなのかなと想像します。
あとは会社のGlobalホームページなどを見ると、いまは全世界で130人以上の従業員が働いているといった記載も見つけることができました。
まだまだ小さな外資系製薬企業です。
でもこの段階の企業が日本に進出してくれるのは珍しいことですね。それは喜ばしいことだと思っています。
KalVista Pharmaceuticals のパイプライン
すでに少しばかり情報が出ていますが、この会社のパイプラインを見ていきます。
こういう情報はGlobalサイトにアクセスするのが一番です。
Pipeline – KalVista Pharmaceuticals | KalVista Pharmaceuticals
2024年4月時点で掲載があるのはこちら。
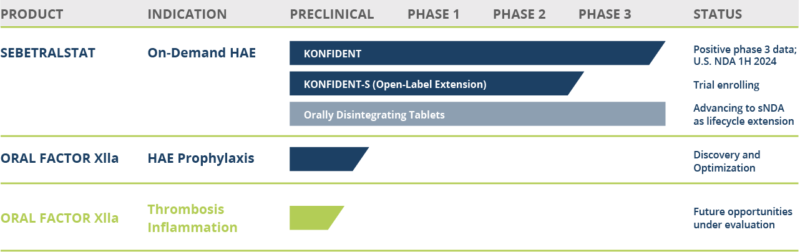
ものになりそうなのは、現時点ではsebetralstatのみですね。
他はまだ前臨床ですので。
このsebetralstatがすでにPh3でPositiveな結果が出ていて、2024年の1HにUSでNDA(New Drug Application):新薬承認申請に進みます。
発売は2025年頃になりそうですね。
株主向けの情報にもアクセスしてみました。
2024年3月11日の最新のプレゼンテーションのリンクを共有しておきます。
Corporate Presentation (kalvista.com)
色々見れます。
ちなみにAIにこの3月11日のプレゼンテーションの要約をお願いをしたら以下のような回答でした。
このPDFの要約は以下の通りです:
- 企業概要: 2024年3月のプレゼンテーションで、経営陣の信念と利用可能な情報に基づいた将来に関する声明が含まれています。
- Sebetralstat: 遺伝性血管性浮腫(HAE)の発作治療用の経口小分子プロテアーゼ阻害剤として開発されており、2024年2月に発表されたフェーズ3 KONFIDENT試験で主要および副次的エンドポイントを達成しました。
- 市場機会: Sebetralstatは、9億ドル規模のオンデマンドHAE市場で初の経口オプションとなり、27億ドル規模の市場全体を変革する可能性があります。
- 財務状況: 2024年2月の公開オファリングで1億6010万ドルを調達し、2026年まで資金が確保されています。
これはPDFの一部の内容に基づいた要約であり、全体的な文脈や詳細を把握するためには、PDF全体を参照することが重要です。もしPDFの特定のセクションについての詳細な要約が必要であれば、教えてください。
リファレンス: ir.kalvista.com
すごい便利ですね、AI。
私はこのPDFの中にある以下の記載が気になりました。
Approved on-demand therapies are injected or infused – high unmet need for efficacious
and safe oral administration
‒ On-demand + prophylaxis is majority share in US, although burden of treatment remains high
‒ On-demand only is majority share ex-US承認されたオンデマンド療法は注射または点滴である。
未充足のニーズが高い2024年3月11日 Kalvista Cooporate Presentation P6
- 米国ではオンデマンド+予防薬のシェアが過半数。
- 米国以外ではオンデマンド療法のみのシェアが過半数
競合薬は注射薬であり、sebetralstatが経口薬であることに大きなチャンスがありそうです。
臨床効果なども、プラセボに比較した時のデータなどが一部掲載されています。
この領域に詳しくないのでこれ以上の説明はやめておこうと思いますが、ご興味ある方はリンクからデータをご覧になってください。
KalVista Pharmaceuticals 日本法人
さて、ここから日本の話に入ります。
まだ日本語のホームページはないようです。
検索すると、2024年1月に法人が設立された情報がヒットします。
KalVista Pharmaceuticals Japan株式会社の本店住所は東京都江東区豊洲6丁目2番31-1917号にあり、法人番号は6010601064511で、設立日は2024年1月です。最新の登記情報では、2024年1月に新規設立または法人番号登録がされました。
KalVista Pharmaceuticals Japan株式会社(東京都江東区)の評判・口コミ・住所・インボイス登録番号・企業情報 | アラームボックス (alarmbox.jp)
日本法人の社長は、アムジェンに買収されたホライゾンの前GMであった沖野さんが2023年9月からお勤めのようです。
Shireや武田にもお勤めの歴が確認できますので、きっとHAEのご経験もあるのでしょうね。
社員数はわかりませんが、プレスリリース情報によると2024年後半に日本で承認申請すると書いてあるので、それに向けて組織を絶賛構築中なのだろうと予想します。
参考:プレスリリース
KalVista Pharmaceuticals の日本で動いている臨床試験
日本の治験はここから確認できます。JRCTのリンクです。
国際共同治験です。
すでに募集は終了してます。
日本の登録は全部で12例
治験施設は
・大阪医科薬科大学病院
・千葉大学医学部附属病院
・群馬大学医学部附属病院
・地方独立行政法人 広島市民病院機構 広島市立広島市民病院
・医療法人 埼友会 埼友草加病院
・公立大学法人 横浜市立大学附属病院
のようです。
すでに試験は終わっています。
そして結果がPositiveであったことも公表されています。
日本は2024年後半の申請に向けて大忙しですね。おそらく。
KalVista Pharmaceuticals の求人情報
Xでのやりとりでマーケティングの案件が動いていることを掴みました。
マーケティングに限らず、R&Dやメディカルもこのタイミングなら動いていると思います。
情報が欲しい方はエージェントさんにコンタクトしてみてください。
・KalVista Pharmaに関してはエンワールドジャパン さんが情報持っているようです。ここは製薬専門チームありです。私もおススメの会社の一つです。
その他、この手の案件で情報を持っているのは、
・JAC Recruitment 外資に行くなら抑えておくべきエージェントさんです。
・Answers 製薬関連の求人数が豊富。製薬ニュースを毎日配信するAnswersNewsと連携してます。
いまはギリアドの案件やリジェネロンの案件もがんがん動いている時期なので、そういう企業に興味ある人は上記エージェントさん達から情報取ったほうが良いです。
以上。
参考になれば嬉しいです!
それでは~





コメント